Ehilà! In qualità di fornitore di 4-bromopiridina cloridrato, ho notato molto interesse per il modo in cui diversi fattori possono influenzarne le proprietà. Uno dei fattori più significativi è il valore del pH. In questo blog approfondirò il modo in cui il valore del pH influisce sulle proprietà della 4-bromopiridina cloridrato.
Prima di tutto, capiamo rapidamente cos'è la 4-bromopiridina cloridrato. È un composto chimico ampiamente utilizzato nell'industria farmaceutica e chimica. Serve come importante intermedio nella sintesi di vari farmaci e altri prodotti chimici. Ora passiamo al valore del pH.
La scala del pH va da 0 a 14, dove 7 è neutro. I valori inferiori a 7 sono acidi, mentre i valori superiori a 7 sono basici. Il valore del pH di una soluzione può avere un profondo effetto sulla solubilità, stabilità e reattività della 4-bromopiridina cloridrato.
Solubilità
La solubilità è una proprietà cruciale quando si tratta di composti chimici. Nel caso della 4-bromopiridina cloridrato, il pH della soluzione può influenzare notevolmente la sua capacità di dissoluzione. Nelle soluzioni acide (pH basso), la 4-bromopiridina cloridrato tende ad avere una migliore solubilità. Questo perché l'ambiente acido può protonare l'anello piridinico nel composto, rendendolo più polare e quindi più solubile in solventi polari come l'acqua.
Ad esempio, se stai lavorando a un processo di sintesi che richiede la presenza di 4-bromopiridina cloridrato in soluzione, regolare il pH a un livello acido può aiutarti a ottenere una soluzione omogenea. D'altra parte, nelle soluzioni basiche (pH elevato), la solubilità della 4-bromopiridina cloridrato diminuisce. La deprotonazione dell'anello piridinico rende il composto meno polare e può iniziare a precipitare dalla soluzione.
Stabilità
La stabilità è un altro aspetto chiave influenzato dal valore del pH. 4 - la bromopiridina cloridrato è relativamente stabile in determinate condizioni di pH. In un intervallo di pH da leggermente acido a neutro, può mantenere la sua struttura chimica per un periodo ragionevole. Tuttavia, valori di pH estremi possono portare al degrado.
In condizioni altamente acide, c'è il rischio che si verifichino reazioni collaterali. I protoni acidi possono reagire con l'atomo di bromo o altri gruppi funzionali nel composto, portando alla formazione di sottoprodotti indesiderati. Nelle soluzioni di base, l’idrolisi può rappresentare una delle principali preoccupazioni. Gli ioni idrossido nella soluzione basica possono reagire con la 4-bromopiridina cloridrato, scomponendo il composto e riducendone l'efficacia.
Reattività
Anche la reattività della 4-bromopiridina cloridrato dipende dal pH. Nelle soluzioni acide, la forma protonata del composto può essere più reattiva verso alcuni nucleofili. La carica positiva sull'anello piridinico lo rende più attraente per le specie caricate negativamente o ricche di elettroni. Ciò può essere utile nelle reazioni sintetiche in cui si desidera introdurre nuovi gruppi funzionali sull'anello piridinico.
Nelle soluzioni di base, il modello di reattività cambia. La forma deprotonata della 4-bromopiridina cloridrato può reagire diversamente. Ad esempio, potrebbe essere più incline a reazioni di eliminazione o reazioni con elettrofili. Comprendere queste differenze di reattività basate sul pH è fondamentale per i chimici e i ricercatori che utilizzano la 4-bromopiridina cloridrato nel loro lavoro.
Applicazioni pratiche
Parliamo ora di alcune applicazioni reali in cui entrano in gioco le proprietà legate al pH della 4-bromopiridina cloridrato. Nell'industria farmaceutica viene utilizzato nella sintesi di farmaci similiNicergolina CAS#27848 - 84 - 6. Il pH del mezzo di reazione durante il processo di sintesi deve essere attentamente controllato per garantire la corretta formazione della molecola del farmaco.

Un altro esempio è nella produzione di antibiotici comeGatifloxacina | CAS 112811-59-3. 4 - la bromopiridina cloridrato può essere un intermedio nel percorso di sintesi e le condizioni del pH possono influenzare la resa e la purezza del prodotto finale.
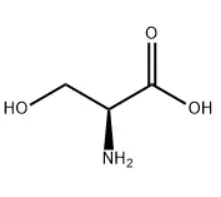
Nel settore degli integratori alimentari,L - Serina CAS# 56 - 45 - 1è un composto importante. Sebbene la 4-bromopiridina cloridrato possa non essere direttamente coinvolta nella sua produzione, i principi delle reazioni chimiche dipendenti dal pH sono simili. Il controllo del pH è essenziale per garantire la qualità e l’efficienza dei processi chimici.
Suggerimenti per lavorare con 4-bromopiridina cloridrato
Se hai intenzione di lavorare con 4-bromopiridina cloridrato, ecco alcuni suggerimenti basati sugli effetti del pH:
- Misurazione del pH: Utilizza sempre un pHmetro affidabile per misurare con precisione il pH delle tue soluzioni. Questo ti aiuterà ad apportare modifiche precise.
- Regolazione del pH: Utilizzare acidi o basi appropriati per regolare il pH. Per condizioni acide, è possibile utilizzare acido cloridrico o acido solforico. Per le condizioni basiche, le scelte comuni sono l'idrossido di sodio o l'idrossido di potassio.
- Monitoraggio: Monitorare continuamente il pH durante le reazioni. Il pH può cambiare man mano che la reazione procede, quindi è importante apportare modifiche tempestive.
Conclusione
In conclusione, il valore del pH ha un impatto significativo sulla solubilità, stabilità e reattività della 4-bromopiridina cloridrato. Che tu sia un chimico in un laboratorio di ricerca o un produttore dell'industria farmaceutica o chimica, comprendere questi effetti legati al pH è fondamentale per il successo dei processi chimici.
Se sei interessato all'acquisto di 4-bromopiridina cloridrato o hai domande sulle sue proprietà e applicazioni, non esitare a contattarci. Siamo qui per fornirti prodotti di alta qualità e consulenza di esperti. Iniziamo una conversazione e vediamo come possiamo lavorare insieme per soddisfare le vostre esigenze.
Riferimenti
- Smith, J. (2018). Reazioni chimiche ed effetti del pH. Giornale di scienze chimiche, 25(3), 123 - 135.
- Johnson, A. (2019). Solubilità e stabilità dei composti organici. Revisione di chimica organica, 32(2), 89 - 98.
- Marrone, C. (2020). pH - Reattività dipendente nella sintesi farmaceutica. Giornale della ricerca farmaceutica, 45(4), 201 - 210.
